Product Quality Review
Regulatorischer Hintergrund
Unterscheidung zwischen Fertigprodukt und Wirkstoff
Der EU GMP Leitfaden unterscheidet beim Product Quality Review zwischen Fertigprodukten (EU GMP Leitfaden Part I Chapter 1.10 / 1.11) und Wirkstoffen (API, EU GMP Leitfaden Part II Chapter 2.6). Für Fertigprodukte sind folgende Punkte in einem Bericht zusammenzufassen:
- A review of starting materials including packaging materials used in the product, especially those from new sources and in particular the review of supply chain traceability of active substances.
- A review of critical in-process controls and finished product results.
- A review of all batches that failed to meet established specification(s) and their investigation.
- A review of all significant deviations or non-conformances, their related investigations, and the effectiveness of resultant corrective and preventive actions taken.
- A review of all changes carried out to the processes or analytical methods.
- A review of Marketing Authorisation variations submitted, granted or refused, including those for third country (export only) dossiers.
- A review of the results of the stability monitoring programme and any adverse trends.
- A review of all quality-related returns, complaints and recalls and the investigations performed at the time.
- A review of adequacy of any other previous product process or equipment corrective actions.
- For new marketing authorisations and variations to marketing authorisations, a review of post-marketing commitments.
- The qualification status of relevant equipment and utilities, e.g. HVAC, water, compressed gases, etc.
- A review of any contractual arrangements as defined in Chapter 7 (EU GMP Leitfaden Part I Chapter 7: Outsourced Activities) to ensure that they are up to date.
Für APIs sind die Punkte 1 (starting materials), 6 (marketing authorization variations), 10 (post-marketing commitments), 11 (equipment qualification status) und 12 (QTA status of outsourced activities) nicht anwendbar und somit werden nur 7 Kapitel gefordert.
Wir bei QuantiValis wundern uns ein bisschen, dass die Punkte 1, 11 und 12 bei den API Herstellern im PQR nicht gefordert werden. In der Praxis sehen wir jedoch, dass viele API Hersteller diese 3 Kapitel freiwillig im PQR integrieren - was wir sehr schätzen.
Die Swissmedic Technical Interpretation zum PQR
Die Swissmedic veröffentlicht technische Interpretationen für die Schweiz zu qualitätsrelevanten Themen rund um die Herstellung und den Vertrieb von Arzneimitteln. Die I-SMI.TI.14e Product quality reviews enthält weitere Informationen zur Erstellung und Evaluierung von PQRs. Besonders interessant finden wir folgende Aspekte:
- der Detailgrad der zu erstellenden Informationen in einem PQR soll risikobasiert und "science based" bestimmt werden. Die Rechtfertigung soll dokumentiert werden.
- auch bei mehreren Zulassungsinhabern (Co-Marketing) sollen alle produzierten Batches in einem PQR dargestellt werden, um eine möglichst hohe Batch Zahl für das Trending zu haben.
- falls es z.B. kleinere Unterschiede in den Spezifikationen des Produktes gibt, soll trotzdem ein PQR erstellt werden mit der jeweils strengsten Spezifikation.
- Verantwortlichkeiten für die Erstellung und Evaluierung von PQRs sollen in einem QTA geregelt werden.
Verlängerung der Review-Periode bis zu 3 Jahren
Falls weniger als 5 Batches in einem Jahr produziert werden, darf die Review-Periode auf bis zu 3 Jahre verlängert werden. Wenn selbst nach 3 Jahren kein einziger Batch produziert wurde, muss trotzdem ein PQR erstellt werden.
Timelines für die Erstellung und Evaluierung von PQRs
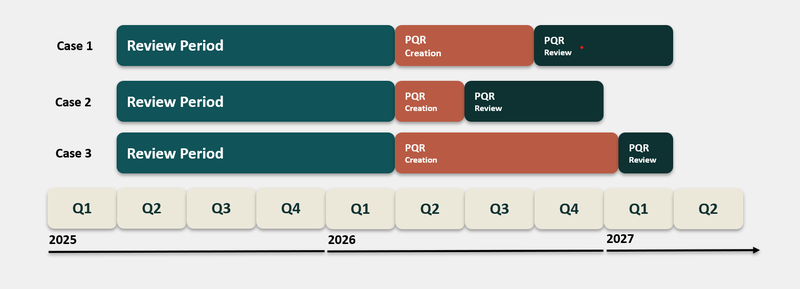
In der Praxis sehen wir, dass insbesondere bei Zulassungsinhabern Verwirrung herrscht. Viele meinen, dass man nach Erhalt des PQRs immer 6 Monate oder sogar bis zu einem Jahr Zeit für die Evaluierung hat. Konkret verstehen wir es aber wie folgt: Der Hersteller hat maximal 6 Monate Zeit für die Erstellung des PQRs. Der Zulassungsinhaber hat maximal 6 Monate Zeit für die Evaluierung des PQR. An folgenden 3 Beispielen soll dargestellt werden, in welchem Fall wie vorgegangen werden soll.
- Case 1: Hersteller braucht 6 Monate für Erstellung, Zulassungsinhaber darf bis zu 6 Monate für Review aufbringen
- Case 2: Hersteller braucht nur 3 Monate für Erstellung, Zulassungsinhaber darf bis zu 6 Monate für Review aufbringen
- Case 3: Hersteller hat hat Verzögerung und braucht 10 Monate, Zulassungsinhaber darf bis zu 2 Monate für Review aufbringen
Ziele eines PQRs
Der Product Quality Review dient der regelmässigen, systematischen Bewertung aller qualitätsrelevanten Daten eines Produktes über einen definierten Zeitraum (in der Regel ein Jahr), mit dem Ziel:
- die Konsistenz und Reproduzierbarkeit des Herstellprozesses nachzuweisen
- die Konformität mit Spezifikationen und Zulassungsunterlagen sicherzustellen
- Trends und potenzielle Risiken frühzeitig zu erkennen
- die Wirksamkeit von CAPAs und Änderungen zu bewerten
- kontinuierliche Verbesserungsmassnahmen abzuleiten
- eine fundierte Grundlage für Managemententscheidungen und Quality Oversight zu schaffen
Brauchen Sie Hilfe für Ihre PQRs?
Wir unterstützen Sie gerne im Bereich PQR, sowohl in der Erstellung als auch in der Evaluierung

